Resumo sobre Alotropia
Trabalho pronto escolar de química sobre Alotropia.
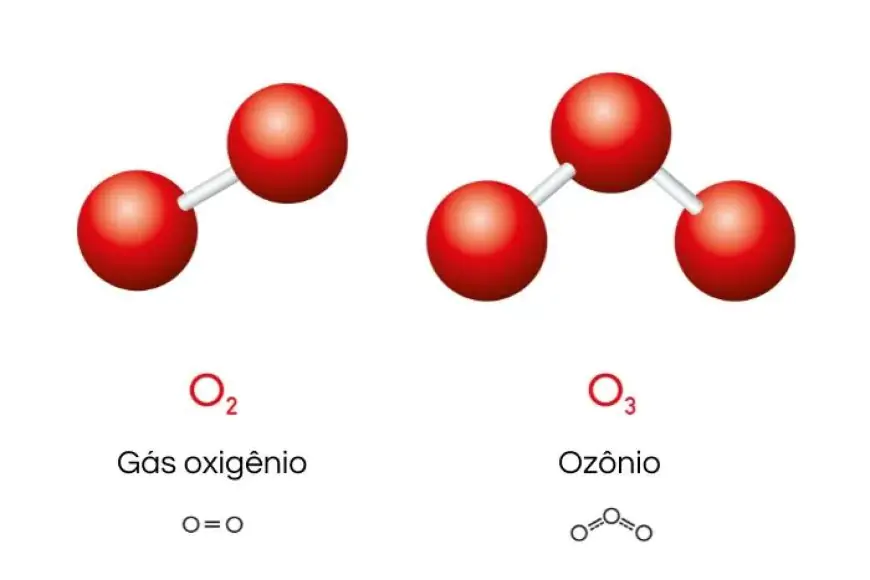
A alotropia ( do grego allos tropos - outra maneira ) é a propriedade que apresentam certos elementos químicos de formarem substâncias simples diferentes. Essas substâncias simples podem apresentar atomicidades diferentes, como o oxigênio ( O2 ) e o ozônio ( O3 ), ou apresentar formas cristalinas diferentes, como o carvão ( que é amorfo ), o grafite ( que apresenta cristais hexagonais ) e o diamante ( que apresenta cristais tetra elétricos ), sendo que todas essas três formas são constituídas exclusivamente de átomo de carbono.
Essas substâncias simples são denominadas variedades alotrópicas ou alótropos do elemento que elas constituem. Os alótropos de um elemento apresentam propriedades físicas diferentes, mas suas propriedades químicas são geralmente iguais.
O ozônio é produzido fazendo-se passar por um arco voltaico entre eletrodos de grafite é a forma alotrópica mais estável de carbono. O diamante é outra forma alotrópica do carbono.
Conclusão: Quando elementos químicos formam substâncias simples diferentes.
Essas substâncias podem apresentar atomicidade diferente como o oxigênio e o ozônio. E formas cristalinas diferentes como o carvão, o grafite e o diamante todas as três são constituídas de carbono.
Essas substâncias são denominadas alótropos.
Os alótropos possuem propriedade física diferente e as propriedades químicas geralmente iguais. O ozônio é produzido um arco voltaico entre eletrodos em atmosfera de oxigênio. O diamante e o grafite são formas alotrópicas.














































































